জলের বৈশিষ্ট্য: আইসোটোপস এবং আণবিক কাঠামো।
জলের বৈশিষ্ট্য 1: সাধারণ
জলের বৈশিষ্ট্য 2: শারীরিক এবং রাসায়নিক বৈশিষ্ট্য
জলের আইসোটপিক রচনা
জল হল নিউক্লিয়াসে প্রোটনের সাথে যুক্ত নিউট্রনের সংখ্যায় অক্সিজেন এবং হাইড্রোজেন আইসোটোপগুলির বিভিন্ন সংমিশ্রণের মিশ্রণ।
1H,2 এইচ (ডিউটিরিয়াম)3এইচ (ট্রিটিয়াম)
16O, 17O,18O.
আইসোটোপিক সম্পর্কগুলি নিম্নরূপ:
হাইড্রোজেনের জন্য:
2H/1এইচ = 1/6900
3H/1এইচ = 1/10 18
ট্রিটিয়াম একটি অস্থিতিশীল উপাদান, এর সময়কাল (অর্ধ-জীবন) 12,5 বছর।
অক্সিজেনের জন্য:
18O/16হে = 1/500
17O/16হে = 1/2500
4 প্রধান আণবিক প্রজাতি এবং তাদের ফ্রিকোয়েন্সিগুলি নিম্নরূপ:
1H216ও = 99,7%
1H2 18 ও = 0,2%
1H217ও = 0,04%
1HD16ও = 0,03%
D216ও = খুব দুর্বল
বিভিন্ন আইসোটোপগুলি অণুগুলির শারীরিক বৈশিষ্ট্যে বিশেষত তাদের ঘনত্বের মধ্যে পার্থক্য আনয়ন করে তবে রাসায়নিক বৈশিষ্ট্যগুলি একই থাকে remain
ভারী জল ডি2ও এর প্রাকৃতিক অবস্থায় রয়েছে তবে খুব আছে
কম প্রশংসনীয় পরিমাণের জন্য, আইসোটোপ পৃথকীকরণের কৌশলগুলি আয়ত্ত করা প্রয়োজন: পারমাণবিক অস্ত্র প্রস্তুত করতে সর্বশেষ বিশ্বযুদ্ধের সময় এটি অন্যতম মৌলিক চ্যালেঞ্জ ছিল।
জলের রাসায়নিক উপাদানগুলির আইসোটোপিক রচনাটি তাপমাত্রার মতো তাপমাত্রা সংক্রান্ত পরামিতিগুলির অনুমানে ব্যবহৃত হয়;
রিপোর্ট 18 O/16O মেরু ক্যাপ থেকে বরফ এবং জীবাশ্ম ভূগর্ভস্থ জল থেকে অতীত জলবায়ু সম্পর্কিত তথ্য সরবরাহ করে।
সমুদ্রের জলের বাষ্পীভবন আইসোটোপিক ভগ্নাংশের সাথে সংঘটিত হয়: অক্সিজেনের হালকা আইসোটোপটি ভারী আইসোটোপকে প্রাধান্য দিয়ে বাষ্পীভবন করে। মেঘের জল এবং বৃষ্টিপাতের চেয়ে সমুদ্রগুলি ভারী আইসোটোপগুলিতে সমৃদ্ধ।
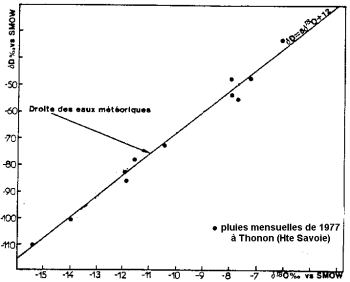
বৃষ্টিপাতের স্থির আইসোটোপ সামগ্রী (ব্লাভাক্স এবং লেটোল, 1995 এর পরে)।
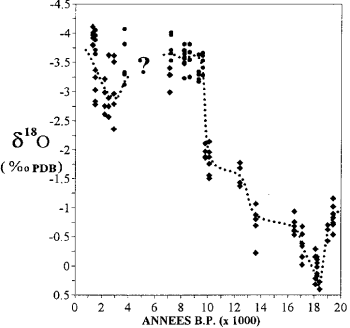
মায়োত্তে প্রবালগুলিতে অক্সিজেন আইসোটোপ সামগ্রীর মধ্যে পার্থক্য (ক্যাসানোভা এট আল এর পরে, 1994)।
অণুর গঠন
হাইড্রোজেন এবং অক্সিজেন পরমাণু তাদের ইলেক্ট্রনগুলিকে নিয়নের মতো একটি সম্পূর্ণ স্তর তৈরি করতে পুল করে। আসলে, অক্সিজেন পরমাণুতে তার বৈদ্যুতিন শেলটি সম্পন্ন করতে 2 টি ইলেক্ট্রনের অভাব রয়েছে, এটি 2 হাইড্রোজেন পরমাণু যা এটি সরবরাহ করে। গঠিত H2O অণু স্থিতিশীল।
অক্সিজেন: 8 প্রোটন + 8 নিউট্রন
হাইড্রোজেন: 2 (2 * (1 প্রোটন + 1 নিউট্রন))
মোট: 10 ইলেকট্রনের চার্জের ভারসাম্যপূর্ণ 10 প্রোটন।
হাইড্রোজেন নিউক্লিয়াকে অক্সিজেনের একপাশে সাজানো হয় একটি বৈশিষ্ট্যযুক্ত "মিকির মাথা" (কান হাইড্রোজেন) form
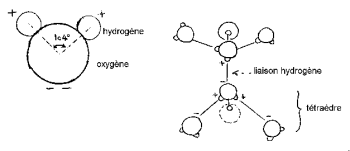
এইচওএইচ কোণ 104,474 ° (টেট্রহেড্রাল জ্যামিতির বৈশিষ্ট্য)। অক্সিজেন এবং হাইড্রোজেন পরমাণুর মধ্যে দূরত্ব বাষ্পের মধ্যে 1 এ ° (0,95718 এ °) এর কাছাকাছি। অণুর কার্যকর ব্যাস হ'ল 2,82 এ order এর ক্রম °
এই ছোট অণুতে বৈদ্যুতিক চার্জ অসমভাবে বিতরণ করা হয়। ইলেক্ট্রন হাইড্রোজেন পরমাণুর চেয়ে অক্সিজেন পরমাণুর প্রতি বেশি দৃ strongly়ভাবে আকৃষ্ট হয়। হাইড্রোজেন নিউক্লিয়াসের নিকটে ইতিবাচক চার্জের 2 টি কেন্দ্র এবং অক্সিজেন নিউক্লিয়াসের নিকটে নেতিবাচক চার্জের 2 কেন্দ্র রয়েছে। চার্জের বিতরণে এই ভারসাম্যহীনতা, জলের অণুটির অ-রৈখিক জ্যামিতির সাথে মিলিত হয়ে একটি শক্তিশালী বৈদ্যুতিক দ্বিপদী মুহুর্তের অস্তিত্বের মধ্যে নিজেকে প্রকাশ করে। জলের অণু পোলার; এটি বৈদ্যুতিন দ্বিপলের মতো আচরণ করে যা এইভাবে অন্যান্য পোলার অণুগুলির সাথে আবদ্ধ হতে পারে। প্রকৃতপক্ষে, জলের অণুগুলি একটি স্ফটিকের গঠন উপাদানগুলির মধ্যে তাদের বিপরীত বৈদ্যুতিক চার্জের অংশটি তাদের দিকে পরিচালিত করে beোকানো যেতে পারে। স্ফটিকের আয়নগুলির আকর্ষণ ব্যাপকভাবে দুর্বল হয়ে যায় এবং স্ফটিকের সংহততা হ্রাস পায়, যা এর দ্রবীভূতিকে সহজতর করে। জলের অণুটির পোলার বৈশিষ্ট্যগুলি মাইক্রোওয়েভ হিটিংয়ের কৌশলটি ব্যাখ্যা করে। আসলে, একটি মেরুকৃত অণু বৈদ্যুতিক ক্ষেত্রের সাথে নিজেকে যুক্ত করে; যদি এটি পরিবর্তিত হয়, অণু ওরিয়েন্টেশন পরিবর্তনের অনুসরণ করে। একটি নির্দিষ্ট ফ্রিকোয়েন্সি থেকে, কয়েক গিগাহার্জ জলের জন্য, অণুর চলাচল ঘর্ষণ দ্বারা তাপ উত্পাদন করে। ঘরের ওভেনগুলি সাধারণত 2,45 গিগাহার্টজ ফ্রিকোয়েন্সিতে পরিচালিত হয় যা ইউএইচএফ।
অণুর 3 টি নিউক্লিয়াস স্থির নয়, তারা একে অপরের সাথে তুলনামূলকভাবে সরানো হয়, অণু স্পন্দিত হয় এবং মোচড় দেয়। তরল জলে অণুগুলি যুক্ত হতে থাকে: মিকির মাথাগুলি হাইড্রোজেন বন্ধন দ্বারা কানকে চিবুক বাঁধে। প্রকৃতপক্ষে, অক্সিজেনের 8 পেরিফেরাল ইলেক্ট্রনের মধ্যে কেবল 4 জন হাইড্রোজেন পরমাণু সহ কোভ্যালেন্ট বন্ধনে জড়িত। বাকি 4 টি ইলেক্ট্রন 2 জোড়া করে ফ্রি ইলেক্ট্রন ডাবল্ট হিসাবে বিভক্ত হয়। এগুলির প্রতিটি নেতিবাচক বৈদ্যুতিক চার্জযুক্ত ডাবল্টগুলি নিকটস্থ জলের অণু থেকে ইতিবাচক চার্জযুক্ত হাইড্রোজেন পরমাণুর সাথে একটি তড়িৎস্তর বন্ধন গঠন করতে পারে। পারিপার্শ্বিক তাপমাত্রায় স্থিতিশীল হাইড্রোজেন তবুও সমবায় বন্ধনের তুলনায় ভঙ্গুর। জলের অণুতে, 2 কোভ্যালেন্ট বন্ড এবং 2 ফ্রি ইলেকট্রনিক ডাবল্টের দিক দিয়ে গঠিত জ্যামিতিটি একটি টেট্রহেড্রনের কাছাকাছি যার কেন্দ্রটি অক্সিজেন নিউক্লিয়ায় দখল করে আছে।
তবে জলের অণুগুলির বৃহত কাঠামো এখনও অপূর্ণভাবে জানা যায়। এক্স-রে এবং নিউট্রন বিচ্ছিন্ন স্পেকট্রা 2 টি মূল মান সরবরাহ করে: 1 এ to এর সাথে সম্পর্কিত একটি সংকেত, হাইড্রোজেন এবং অক্সিজেন নিউক্লিয়াসের মধ্যে দূরত্ব এবং তাপমাত্রা অনুসারে 2,84 থেকে 4 এ-এর মান পরিবর্তিত হয় and 2 অক্সিজেন নিউক্লিয়াসের মধ্যে দূরত্বের সাথে সম্পর্কিত। এক্স-রে ডিফ্র্যাক্টমিট্রি প্রদত্ত অণু থেকে একটি দূরত্বে অবস্থিত তরলটির প্রতি ইউনিট ভলিউমের গড় সংখ্যারও জানা সম্ভব করে তোলে। একটি জলের অণুতে গড়ে গড়ে ৪.৪ প্রতিবেশী থাকে, যা একটি টিট্রেহেড্রাল জাল প্রস্তাব করে। হাইড্রোজেন বন্ড দ্বারা যুক্ত অণু ছাড়াও, অন্যান্য আনবাউন্ড অণু রয়েছে, যা ব্যাখ্যা করতে পারে যে প্রতিবেশী অণুগুলির সংখ্যা 4,4 এর চেয়ে কিছুটা বেশি কেন, এবং 4 টি ঠিক কড়া টেটারহেড্রাল স্ফটিকযুক্ত রাষ্ট্রের প্রয়োজন অনুসারে নয়। হাইড্রোজেন বন্ধনের সাথে সংযুক্ত অণুগুলির স্ফটিক জালগুলি গহ্বর তৈরি করে যেখানে আনবাউন্ড অণুগুলি রাখা হত। আরেকটি অনুমান হাইড্রোজেন বন্ধনের বিকৃতির উপর ভিত্তি করে। পরেরটি, মূলত রৈখিক, এটি ও - এইচও পারমাণবিক প্রান্তিকের সাহায্যে বলা যায়, এটি বিভিন্ন ডিগ্রিগুলিতে মোচড় দিতে পারে এবং নিকটবর্তী প্রতিবেশীদের চেয়ে দূরবর্তী অণুগুলিকে কেন্দ্রীয় অণুতে যেতে দেয়।
তাত্ত্বিক মডেলগুলি সম্প্রতি শক্তিশালী কম্পিউটার ব্যবহার করে তৈরি করা হয়েছে। তারা নির্দেশ করে যে প্রায় 80% জলের অণু 3 বা 4 হাইড্রোজেন বন্ধনে জড়িত; অন্যদিকে, তারা আনবাউন্ড অণুগুলির উপস্থিতি বাদ দেয়। কম্পিউটার মডেলিং পরামর্শ দেয় যে জল ঠাণ্ডা হওয়ার সাথে সাথে অণুগুলির নেটওয়ার্কগুলি ক্রমশ বরফের মতো হেক্সাগনগুলির সাথে সাদৃশ্যপূর্ণ।
শক্ত রাষ্ট্রটি একটি কঠোর স্ফটিকের বিন্যাসের সাথে মিলে যায়। সাধারণ চাপে, বরফের একটি ষড়ভুজ কাঠামো থাকে। নিম্ন তাপমাত্রায় (-80 ° C এর নিচে), এটি একটি ঘন কাঠামো নিতে পারে। বৈদ্যুতিক চার্জগুলি স্ফটিক জালাগুলিতে সরে যেতে পারে এবং আয়নিক ধরণের স্ফটিক ত্রুটিগুলি তৈরি করতে পারে: হাইড্রেটেড প্রোটন এইচ 3 ও + এবং হাইড্রোক্সিল আয়ন ওএইচ-। বরফের স্ফটিক জালটি অণুর সর্বাধিক কমপ্যাক্ট স্ট্যাকিংয়ের সাথে মিলে না। সংশ্লেষণে, ত্রুটিগুলি হ্রাস পায় কারণ হাইড্রোজেন বন্ধনগুলি ভেঙে যায় এবং অণুগুলি একত্রে কাছাকাছি আসে: ঘনত্ব সর্বোচ্চ 4 ডিগ্রি সেন্টিগ্রেডে বৃদ্ধি পায় increases পরবর্তীকালে তরল জলে তাপমাত্রা বৃদ্ধি অণুগুলিকে আলাদা করে দেয় এবং ঘনত্ব হ্রাস পায়।
আরও তথ্যসূত্র এবং গ্রন্থপঞ্জি সন্ধান করুন:
ব্লাভাক্স বি এবং লেটোল আর। (1995) - ভূগর্ভস্থ জলের জ্ঞানের ক্ষেত্রে আইসোটোপিক কৌশলগুলির অবদান। জিওক্রোনিক্স, 54, পি। 12-15।
ক্যারো পি। (1990) - জলের শারীরিক এবং রাসায়নিক বৈশিষ্ট্য। জলের দুর্দান্ত বই, লা ভিলেট, পি। 183-194।
ইগল্যান্ড ডি (1990) - জলের কাঠামো। গবেষণা, 221, পি। 548-552।
পরিচারিকা ডিআর (1992) - হাইড্রোজোলজির হ্যান্ডবুক। ম্যাক গ্রু হিল
ক্যাসানোভা জে।, কর্ননা এম এবং জেরারউড কে। (1994) - জিওপ্রোস্পেক্টিভ - পেলিয়োক্লিম্যাটোলজি। র্যাপ। বিজ্ঞানী। বিআরজিএম, পি। 76-79।

